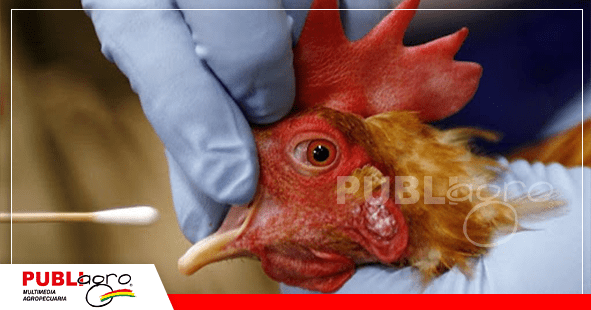
Detectar niveles relativos de anticuerpos y evaluar la respuesta a la vacunación permite tomar decisiones más precisas en el manejo de la parvada
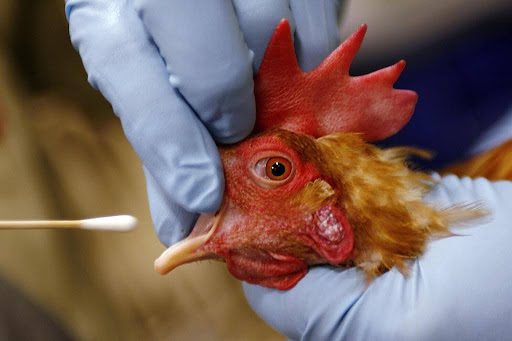

La interpretación de los resultados de una prueba ELISA requiere atención a varios aspectos fundamentales para garantizar que los resultados sean fiables y clínicamente útiles. Uno de los primeros puntos a considerar es la revisión constante del estado inmune de la parvada y la detección oportuna de la aparición de patógenos, factores esenciales para la planificación sanitaria de cualquier granja avícola.
Según Fernando Acuña, director técnico de LATAM Biochek, “una de las preguntas importantes es si se ha vacunado correctamente la población, monitoreando y si se han cumplido los desafíos de campo”. Esta observación subraya la relevancia de contar con programas de vacunación bien estructurados y un seguimiento riguroso de la respuesta inmunitaria de las aves.
Existen diferentes tipos de pruebas ELISA, como la directa, indirecta, de captura (sandwich) y competitiva, cada una con características específicas que determinan cómo se detecta el analito y cómo se interpretan los resultados. Por ejemplo, las pruebas tipo sandwich se utilizan especialmente para la detección de antígenos, mientras que las pruebas indirectas son más comunes para la identificación de anticuerpos.
Los resultados de una prueba ELISA se obtienen midiendo la densidad óptica (DO) de cada muestra en un espectrofotómetro, comparándolos con los controles positivos y negativos incluidos en cada kit. Además, cada prueba cuenta con un valor de corte, que permite clasificar las muestras como positivas, negativas o dudosas. Según los resultados, las muestras pueden interpretarse de la siguiente manera:
- Positivo: se detecta la presencia del anticuerpo o antígeno específico.
- Negativo: no se detecta el analito buscado.
- Indeterminado o dudoso: se recomienda repetir la prueba o confirmar mediante métodos complementarios.

“Cuando hacemos un PCR lo que estamos evidenciando directamente material genético específico del patógeno que se sospecha que está infectando a los animales. A diferencia de las pruebas serológicas, que identifican la respuesta inmune (anticuerpos), el PCR permite evidenciar directamente la presencia del virus, bacteria o parásito en la muestra”

Existen factores que pueden afectar la interpretación de los resultados, como falsos positivos, que pueden generarse por reacciones cruzadas con otros antígenos, y falsos negativos, que pueden ocurrir por concentraciones bajas del analito o errores en la manipulación de la muestra. Asimismo, el momento de la toma de la muestra es crucial, ya que, especialmente en pruebas serológicas, si se realiza antes de que las aves generen suficientes anticuerpos, el resultado puede ser negativo.
En definitiva, la correcta aplicación de los programas de vacunación permite justificar la inversión en salud avícola y facilita un control adecuado mediante monitoreo serológico.
En relación con las pruebas moleculares, Acuña explica:
“Cuando hacemos un PCR lo que estamos evidenciando directamente material genético específico del patógeno que se sospecha que está infectando a los animales. A diferencia de las pruebas serológicas, que identifican la respuesta inmune (anticuerpos), el PCR permite evidenciar directamente la presencia del virus, bacteria o parásito en la muestra”.
Mientras que el ELISA detecta una respuesta secundaria al paso de ese patógeno, ya sea celular o de cualquier organismo vivo, el PCR identifica de manera directa la presencia del agente infeccioso.
Es importante señalar que, aunque se suele pensar que ELISA es una prueba cuantitativa, en realidad se trata de una prueba semicuantitativa, ya que detecta niveles relativos de anticuerpos y no la cantidad exacta de estos. Esto significa que proporciona un valor relativo, útil para comparar respuestas entre animales o grupos, pero no determina con precisión la concentración absoluta de anticuerpos.
En conclusión, interpretar correctamente una prueba ELISA no depende únicamente del valor numérico de absorbancia, sino de considerar el tipo de prueba, los controles, el valor de corte y el contexto clínico, lo que garantiza decisiones más seguras y confiables en el diagnóstico y seguimiento de las aves.

Fuente: Fernando Acuña
Redacción: Publiagro